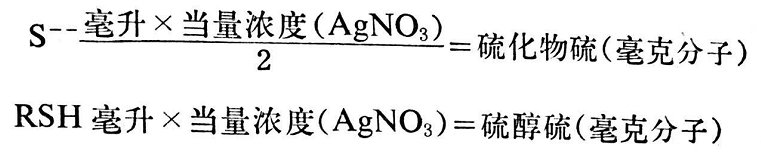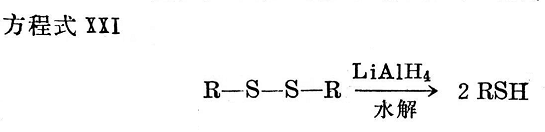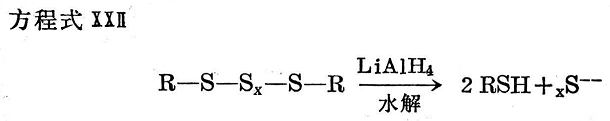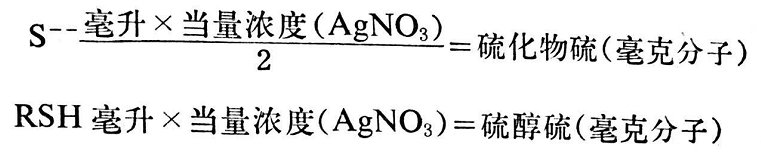3.1.3.2四氫化鋰鋁法
3.1.3.2.1方法原理
M.L.塞爾克和A,R.肯普的方法屢次受到非議。應(yīng)該說明,不僅是分子間的鍵合硫與碘甲烷反應(yīng),而且分子內(nèi)鍵合的(環(huán)化)硫同樣能夠進(jìn)行反應(yīng)。這就會(huì)導(dǎo)致虛假的結(jié)果。M.L史蒂倍克和L.G.內(nèi)伯斯(L.G. Nabors)510以及C.G.穆爾10也都說過,碘甲烷法得到的結(jié)果非常難以解釋。但其結(jié)果清楚地表明,例如在膠料用二硫化秋蘭姆作無硫硫化時(shí),得到的不是硫交聯(lián)鍵便是C一C交聯(lián)。如不存在C一C交聯(lián)鍵時(shí),則用氫化鋰鋁進(jìn)一步辨別單硫鍵雙硫鍵和多硫鍵,便特別簡單0。在G.A斯坦馬克(G.A. Stenmark)和F,T.韋斯(F.T. Weiss)510p以及R.C.阿諾德(R.C. Arnold)、A.P.利恩(A,P.Lien)和R.M.阿爾木(R.M.Alm)5109等人的文章中,有關(guān)于應(yīng)用氫化鋰鋁的報(bào)道。通過氫化鋰鋁的作用,單硫鍵保持不變,但雙硫鍵被水解而形成硫醇,見方程式X。方程式XXI。
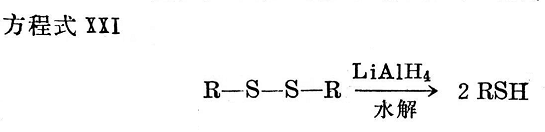
另一方面,當(dāng)多硫鍵與氫化鋰鋁反應(yīng)時(shí),它們給出硫醇和與其本身相當(dāng)?shù)牧蚧锪浚姺匠淌絏XⅡ。
從還原樣品所形成的硫醇和硫化物,可用電位滴定測定。多硫化物用檢出的硫化物數(shù)量表示。X所代表的數(shù)值可用苯膦作試劑確定。根據(jù)測定的多硫交聯(lián)鍵數(shù)與總的斷裂鍵數(shù)之差,即可得到雙硫鍵。還原后仍然保留的交聯(lián)鍵數(shù)和原來總數(shù)之差(假定沒有C一C交聯(lián)鍵)代表單硫交聯(lián)鍵數(shù)。
3.1.3.2.2分析步驟
分析樣品的制備:
取1. 5克的硫化膠薄片置索格利特抽提器中用氯仿抽提7天,而后在真空中于室溫下千燥24小時(shí)。隨后將樣品在75亳升純乙醚中煮沸并回流1小時(shí)。加入10毫升濃鹽酸,然后將氮?dú)馔ㄈ敕磻?yīng)瓶。再將樣品回流四小時(shí)。形成的硫化氫在酸性醋酸鎘水溶液中吸收。然后用碘量法測定硫化物的硫。將過量的乙醚和鹽酸傾析之后,用蒸餾水洗滌樣品并進(jìn)行干燥。然后用純甲醇抽提48小時(shí),再在室溫下通氮干燥48小時(shí)。
這時(shí),將取出的樣品包在石蠟中,用切片機(jī)切成薄片,并用50毫升的正己烷將石蠟除去。再用20毫升正己烷將這些薄片引入125毫升的三口燒瓶內(nèi),中間裝置一冷凝管,一邊裝通氮毛細(xì)管,另一邊裝一滴液漏斗用以添加試劑。
試劑:
醋酸鎘溶液:25克醋酸鎘和100毫升冰醋酸加入875毫升蒸餾水中。
反應(yīng)溶液:180毫升通過氫化鋰鋁精餾之四氫呋喃和18克氫化鋰鋁在一起攪拌,過夜,并通過玻璃棉過濾。然后加入三滴下面所講的指示氫化鋰鋁的指示劑溶液。
指示劑溶液:1%的4-苯偶氮基一二苯胺的苯溶液。硝酸銨乙醇溶液:5克硝酸銨溶于1升蒸餾變性乙醇中。
還原操作:
盛有正己烷和樣品的反應(yīng)容器,用氮很好地凈化并在冰浴內(nèi)冷卻。加入30毫升的四氫呋喃。該溶液已通過氫化鋰鋁精餾并含有足量氫化鋰鋁而使指示劑呈淡褐色。然后滴加3毫升反應(yīng)溶液。一開始反應(yīng)緩慢,隨后速度加快。反應(yīng)溶液的加入速度,應(yīng)能使反應(yīng)約在5分鐘以后結(jié)東。然后反應(yīng)容器置于25°0的水浴上,并用磁攪拌器攪拌3小時(shí)。再加10毫升硝酸銨乙醇溶液將過量的氫化鋰鋁分解。這種溶液一開始是用滴加的辦法加入的,至氫的產(chǎn)生比較明顯時(shí),即攪拌加入其余的溶液。最后加入3毫升濃氫氧化銨,并用20毫升硝酸銨乙醇溶液凊洗。燒瓶內(nèi)的物質(zhì)倒入250毫升的燒杯內(nèi),再用70亳升硝酸銨酒精溶液洗滌燒瓶。
滴定(電位滴定):
溶液以0.1N的硝酸銀溶液滴定(如用俄亥俄州 Cleveland微量儀器公司生產(chǎn)的SB-2注射徽量滴定管)。可用銀一氯化亞汞體系作電極。接近終點(diǎn)時(shí),約用每分鐘一滴的速度滴入硝酸銀。電位的毫伏數(shù)用電位計(jì)測定。若有硫化物的分解產(chǎn)物的時(shí)候,電位計(jì)指示值在450和600毫伏之間,而有硫醇基分解產(chǎn)物時(shí),其值在150和330毫伏之間。硫化物分解產(chǎn)物可以很快地滴定,而硫醇基分解產(chǎn)物需要較長的時(shí)間才能達(dá)到平衡。